第2部 凍結組織検体の適切な採取・保管・移送方法
DNA・RNA・タンパク質等の変性を最小限にし、高い品質を保持して長期の保管を可能にし、将来に亘って広汎な解析に供せるよう汎用性を最大にすることを目指し、ゲノム研究等に供する病理凍結組織の適切な取扱い方法を定める。
凡例
- (E)
- (A)よりもさらに高い品質等が期待できる場合があるが、作業量が過大である等のため、必須とは言いがたい事項
- (A)
- 推奨される事項
- (B)
- (A)が実施不可能である場合に次に推奨される事項
- (N)
- 回避すべき事項
- (L)
- 法令等により規定されている事項
【採取対象】
- 第1部「研究用病理組織検体の適切な採取部位」の記載の通り、手術標本より、病理診断に支障を来さず (患者に不利益を及ぼさず)、核酸・タンパク質等の変性の予測される 出血・壊死巣等を回避し、適切な採取部位よりゲノム研究等に用いる組織検体を採取する (A)。
注: 包括的同意等に基づくバイオリソースバンキング等に際して、生検標本を診療後余剰検体と見なしがたい場合が多いと考えられる。そこでまず、手術標本より採取したゲノム研究等に用いる組織検体の取り扱いについて定める。
注: 個別同意に基づく場合等、生検標本をゲノム研究等に用いる場合は、本規程第2部【急速凍結】16. 以降に準拠して扱う。
- 例えば、癌症例であれば、癌部と非癌部(適切な対照部位)の双方から検体を採取する (A)。(第1部 6. 採取部位の決定参照)
注: 一般に癌組織にはheterogeneityがあるが、肉眼所見に不均一性が認められる場合等は特に、癌部の複数箇所から組織を採取することが望ましい (E)。
- 採取部位について最低限の記載を残すべきである (A)。
例 体部小弯側
注: 写真・シェーマへのおおよその部位の記入、近接する部位より作成したルーチンの病理診断等のための ブロック番号の記録、等の手段により、採取部位に関する情報が研究者に伝達されるように計らうこともさらに望ましい (E)。
注: 病変部の複数箇所から組織を採取した場合等においては、特記すべき肉眼所見の文章による記載等を行うこともさらに望ましい (E)。
【採取者】
- 各症例の手術標本において、組織検体の採取の可否、適切な採取部位、適切な採取組織量を、望ましくは病理専門医が判断する(E)。あるいは、病理診断学に精通し、充分な肉眼病理診断能力を備えた、担当診療科等の臨床医が判断することも望ましい (A)。
- 研修医・臨床検査技師・その他のバイオバンク実務者が採取を行う場合には、ゲノム病理標準化センター講習会ならびに日本病理学会webページにおけるe-ラーニングシステム等で研修を行った上で、第1部「研究用病理組織検体の適切な採取部位」の記載に従い、また必ず病理専門医あるいは病理診断学に精通した担当診療科等の臨床医の監督の下で採取を行う (B)。
【採取時間】
注: 手術検体が手術標本整理室等に提出されたのち、入割・肉眼診断・写真撮影等のかたわら組織検体の採取を行う場合、最も速やかに作業すれば、【急速凍結】16.までを摘出後30分以内に実施できると考えられる。
注: 手術検体を室温で長時間保持することは極力回避する(N)。[実証データ ①]・[実証データ ②]
注: 最終的に得られた核酸等の品質は、バイオバンクの採取・保管条件よりも、提供を受けた研究者側の手技に依存する場合がある。[実証データ ③]
- バイオバンク等から研究者に試料を提供する際に、時間・温度等の項目を含む、当該施設における標準手順書を開示する必要がある (A)。また、当該施設における標準手順を逸脱した場合は、試料付随情報に、時間・温度等逸脱した事項の記録を含める必要がある(A)。
注: 採取時間あるいは摘出後採取までの所要時間・採取までの保持温度は、正確に記録することが望ましいが、当該施設における標準手順に従って採取している限りは、試料の質の予測が可能であるので、時間・温度の記録は全症例において必須ではない (E)。標準手順を逸脱した場合は、上記8.のように対処する。
注: 診療録等を閲覧して当該症例の 術中疎血時間を記録する労力は研究における必然性に鑑みて過大であり、全症例において必須ではない (E)。ただし、試料が疎血時間の影響を受けやすい解析を含む研究に供される等、研究者の求めがある場合には、疎血時間を開示できる体制をとることが望ましい (A)。
【採取量】
- 採取量については4.に示した通り病理専門医あるいは病理診断学に精通した担当診療科等の臨床医の判断によるが、病理診断に特段の支障がなく適切な採取部位が確保できる場合は、半小指頭大 (1×0.5×0.3cm 程度、50mg-100mg程度)の組織を採取することが適切である (A)。
注: 極少量の組織を用いても有益な解析を行う余地があるので、採取量が半小指頭大に満たないことを持って、採取を見合わせるにはあたらない (B)。
注: 組織の湿重量による補正等が必要となる解析を行う可能性が高い場合には、精密計量器をもって採取組織の湿重量を測定することが望ましい。但し、秤量作業により急速凍結までの時間が遅延する弊害があり、細切した個々の組織片が研究者に提供されるため、採取全量の秤量は必ずしも研究者を利するとは限らない。細切した個々の組織片毎の秤量は、急速凍結までの時間を更に遅延させる。よって湿重量の秤量を、必須要件とはしない (E)。
【組織の処理】
- 9.で採取した組織を1 辺 2-3mm 角程度にまで細切する(A)。
注: 使用細片以外の凍結・融解の反復を防ぎ、核酸分解酵素等の活性化を防いで速やかに質の高い解析を行うため、急速凍結前の組織の細切は必須である (A)。
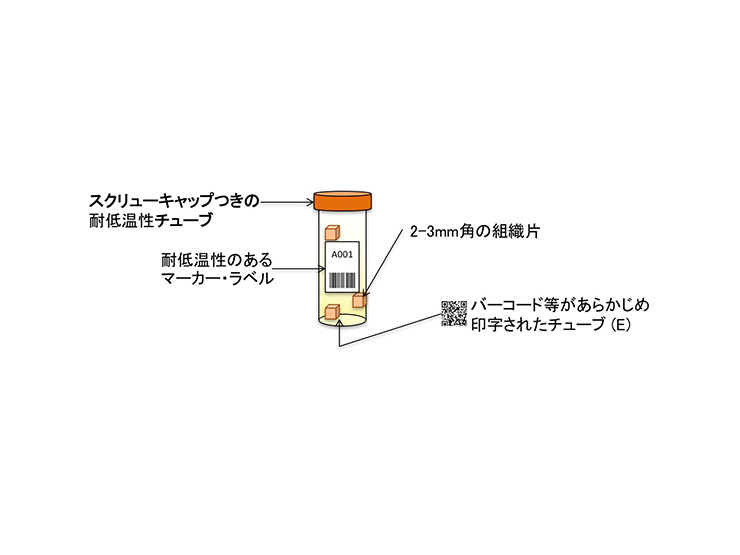
- 望ましくは、2-3mm角組織片1個を1チューブに収納する(E)。保管容器の容量に制限がある場合には、チューブの内壁に個々の組織片を相互に離して貼付するようにし、複数の組織片を1チューブに収納する (A)。
注: チューブの内壁に相互に離して貼付しておけば、使用時に、残りの組織片を含めたチューブ全体の温度が上昇するより先に、必要個数のみ鑷子等で素早く引き剥がすことができる。
注: 複数の組織片を1チューブに収納する場合は、1.5mlないし2mlの容量のチューブが扱いやすいが (A)、組織片1個を1チューブに収納する等の場合はこの限りでない。
- 耐低温性のあるチューブを用いる (A)。匿名化番号等をチューブに記載するか貼付する場合、耐低温性のあるマーカー・ラベル等を用いる (A)。
注: チューブ・マーカー・ラベル等は、各施設の保存庫等で実際に耐低温性を確認してから採用することが望ましい (E)。
注: 各施設の管理体制に応じて、匿名化番号のバーコード等があらかじめ印字されたチューブを用いることも推奨される (E)。
- 万一の温度変化に備える (液体窒素の膨張による事故を防ぐ) ため、スクリューキャップつきのチューブを用いる (A)。
- 癌部・非癌部等各採取部位から、11.のチューブを複数本作成する (A)。
注: 複数の組織片を1チューブに収納している場合にも、複数箇所に保管したり、複数の研究者への提供を行う便等を考え、必ず複数本のチューブを作成する (A)。
注: 各施設等において合意が得られた場合、また特に液体窒素保存容器中で高い品質を維持して保管が可能である場合、解析手技が進歩した将来における研究使用に備えて、複数採取したチューブの一部を特に長期保管する (例として10年以上等)ことも望ましい (E)。
- 核酸庇護剤が多種類市販されており、チューブ内において核酸庇護剤に組織片を浸漬して凍結する手技が多用されている。但し、核酸の質を確実に保持するとともに、試料の汎用性を高めるため、可及的に速やかな組織の採取と急速凍結が可能な施設においては、核酸庇護剤を使用しないことも推奨される。
注: 核酸庇護剤中で凍結した組織を核酸抽出手技に供した場合、DNAの品質は概して影響を受けない。[実証データ ④]
注: 核酸庇護剤の種別により、RNAに対する効果にはかなりのばらつきがある。核酸庇護剤を使用しようとする場合は、各施設において実際に核酸を抽出して品質を検証した上で、適切な核酸庇護剤を選択するべきである。[実証データ ⑤]
注: 核酸庇護剤中で凍結した組織を核酸抽出手技に供した場合、核酸庇護剤を用いずに凍結した組織から核酸を抽出する場合に比して、核酸庇護剤の融解を待つ工程が増える等するため、抽出したRNAの品質がかえって低下する場合がある。[実証データ ⑤]
【急速凍結】
- 14.で複数本ずつ作成したチューブを液体窒素に浸漬し、急速凍結を行う (A)。6.で述べたように、最も望ましくは、手術標本摘出後30分以内に急速凍結を実施する (A)。
注: 液体窒素を容れたコルク栓付きデュワー瓶 (2重壁断熱容器)等にチューブを浸漬して急速凍結する (A)。

注: 頻繁に (連日多数の)試料を採取する施設においては、容量30ないし50リットル程度の比較的小型の急速凍結用液体窒素保存容器を、新鮮未固定の手術標本を扱う手術標本整理室等に常設し、14.で作成したチューブを速やかに収納して急速凍結を行うのが効率的である(E)。この場合、充分凍結した試料を定期的に長期保管場所までまとめて運搬することが出来る。

注: 手術標本整理室等において液体窒素の調達が困難である施設では、ドライアイス・アセトン等による凍結が可能である (B)。[実証データ ⑥]・[実証データ ⑦]
注: 手術標本整理室等において液体窒素の調達が困難であるが、手術標本整理室内に超低温槽(-80℃)を常設できる施設においては、超低温槽(-80℃)に速やかにチューブを収納することも可能である (B)。[実証データ ⑥]・[実証データ ⑦]
【長期保管】
- 16.で急速凍結したチューブは、最も望ましくは、研究使用に供すまで液体窒素保存容器(-180℃程度)に保管する(A)。
注: ここで「長期保管」とは、研究使用に供すまでの期間保管することをさすが、一般的に5ないし10年以上の保管を期して設備・標準手順を定めるべきである。
注: 標準的には液相の液体窒素保存容器を用いる (A)。 保管場所等が確保できる場合には、病原微生物のコンタミネーションを避ける等の観点から、アイソサーマル式等全面気相の液体窒素保存容器を用いることが更に望ましい (E)。但し、大型で設置に高額の経費を要するため、気相の液体窒素保存容器の導入の是非は施設の判断による。
注: 長期保管場所までの施設内搬送にも、液体窒素を容れたコルク栓付きデュワー瓶(2重壁断熱容器)等、熱伝導率が小さい十分断熱性能を備えた容器を使用する。
注: 長期保管のため液体窒素保存容器に収納する等の作業は、通常用手的に行うが、試料の温度変化を最小限にするため、極力手早く行うものとする(A)。
注: チューブに印字された匿名化番号バーコード等を識別し自動出入庫を行うシステムを備えた液体窒素保存設備等を用いることも、屋外大型貯槽ならびに液体窒素の自動供給システムを備えた液体窒素保存設備等を用いることも、品質保持と省力化の観点から更に望ましい (E)。 但し、大型で設置に高額の経費を要するため、長期保管設備は各施設等の判断に基づいて選択するものとする。
- 長期保管のため液体窒素保存容器に収納するとともに、試料の付随情報・保管場所等を、適切な管理アプリケーション・カタログデータベース等に登録する (A)。
<参考>バイオバンク実務者等がカタログデータベース入力する際の原資料とするため、試料採取者に対して試料と共に提出する“試料登録票”等に標準的に記載を求める項目は以下の通りである。(誤入力を防ぐために、試料採取者による発生源入力のデータベースを構築することも望ましい。)
- ①手術 (採取)年月日: 西暦年月日、病理IDが未発番の場合、同一患者の複数回の手術を区別するために必須である。
- ②試料採取者: 試料を用いた研究の共同研究者となり、バイオバンクからの払い出し可否を判断する、バイオバンクコンタクトパーソン等 [担当病理医、各診療科の臨床医等]が決められている場合、その氏名を記載する。
- ③患者氏名: カタログデータベースに合致するよう、カタカナ姓名、漢字姓名、あるいはその両者等書式を指定する。
- ④患者ID
- ⑤病理ID: 検体採取時にすでに発番されている施設においては、同一患者の複数回の手術を区別するために記載を求める。
- ⑥提出診療科: 提出診療科はカタログ検索キーワードになりうるので、誤記入を防ぐために、あらかじめ全診療科名を列記し、その中から選択することを試料採取者に求める。
- ⑦感染症: 試料管理・研究利用に際し確認の必要な診断名をあらかじめ列記し、その中から選択することを試料採取者に求める、“その他”の項に自由記載を許す。
- ⑧性別: 電子カルテと連動したバイオバンクのカタログデータベースが完備され、患者IDから自動入力できる施設においては必須ではない。
- ⑨手術 (採取)時年齢: 研究使用時等には、電子カルテ等から採取当時の年齢を自動抽出しにくいので、採取時に記載を求める。
- ⑩臨床診断:自由記載、カタログにおいては部分一致検索等に用いる。
但し、正確な診断名からの検索を可能にするには、病理診断確定後にバイオバンクのカタログデータベースを電子カルテ・院内がん登録等に連動させ、ICD10コード・MEDIS管理番号等から検索できるようにする必要がある。 - ⑪採取臓器: 試料管理に際し分類収納等に用いる可能性がある場合、自由記載は不可とし、あらかじめ臓器名を列記しておき、その中から選択することを求める。WHO 腫瘍分類臓器コード等を用いても良い。
- ⑫チューブ本数: T (癌部・病変部)◯本、N (非癌部・対照部)◯本。
- ⑬試料付随情報
- T1: 採取部位 (例 体部小弯側、ブロック番号#、採取部位を記入した臓器写真・シェーマも添付できるようにする)。肉眼所見等の自由記載も許す。
- T2: 同様に採取本数分の記載を求める。
- N1: 採取部位 (例 体部小弯側、ブロック番号#、採取部位を記入した臓器写真・シェーマも添付できるようにする)。肉眼所見等の自由記載も許す。
- N2: 同様に採取本数分の記載を求める。
- ⑭施設の標準手順から逸脱: “あり”・“なし”より選択する。ありの場合状況説明の自由記載とするが、摘出後実際に凍結までに要した時間と凍結まで臓器を保管した温度 (室温、4℃等)を必ず記載に含めるよう求める。
- ・以下は、施設の標準手順から逸脱していない場合必須ではないが、施設内でコンセンサスが得られ無理なく記載できる場合に記載してもよい。
- -摘出時間(24時制◯時◯分)、 採取凍結時間(24時制◯時◯分) あるいは
摘出後凍結までの時間 (約◯分) - -術中阻血時間 (約◯分)
- -湿重量 (◯mg)
- -摘出時間(24時制◯時◯分)、 採取凍結時間(24時制◯時◯分) あるいは
- ・以下は、施設の標準手順から逸脱していない場合必須ではないが、施設内でコンセンサスが得られ無理なく記載できる場合に記載してもよい。
- 長期保管に、液体窒素保存容器 (-180℃程度)にかえて、超低温槽 (-80℃)を用いることも可能である(B)。この場合も、望ましくは16.に述べたように液体窒素に浸漬して急速凍結し、手早く超低温槽に収納する(A)。
注: 超低温槽 (-80℃に組織を長期保管したのち抽出したDNA・RNA・タンパク質の品質は、液体窒素保存容器に長期保管した組織から抽出したそれらに比べて、低下する場合がある (DNA・RNAについていえば、特に10年以上経過したのち品質が低下する場合がある)。 [実証データ ⑧]・[実証データ ⑨]・[実証データ ⑩]
注: 汎用性を高めるために液体窒素保存容器中の長期保管が推奨されるが、-80℃に長期保管した組織から抽出したDNA・RNAを用いても、特段問題なく実施できる解析項目は多いので、実行可能性にも鑑みて長期保管温度は各施設等の判断に基づいて選択するものとする (B)。試料を利用する研究者は、保管試料の品質に応じた適切な解析項目を選択するべきである (A)。このため、[実証データ ⑧]・[実証データ ⑨]・[実証データ ⑩]を参照されたい。
- 長期保管に、冷凍庫 (-20℃)を用いることは回避すべきである (N)。
- 試料を提供するバイオバンク等の施設は、保管試料の特性・品質に関する情報を研究者に提供する目的で、バイオバンク試料を用いた利活用研究の成果 (刊行論文等)を適宜webページ等で公開することが望ましい (A)。
- 試料を提供するバイオバンク等の施設が、少数の試料について定期的に抜き取り実証解析等を行い、結果を公表することはさらに望ましい (E)。全試料において核酸のintegrityを示す指標を実測し、公開・添付して試料を提供することがさらに望ましいが、実行可能性に鑑みて必須とは言えない (E)。
- 長期に亘る保管期間中の故障・事故等の可能性を考慮し、可能であれば温度管理記録を残すことが推奨される (E)。
- 長期に亘る保管期間中の事故・災害等の可能性を考慮し、バックアップとするために、可能であれば遠隔地の別施設等に分散して保管することも望ましい (E)。
【凍結組織切片作製】
- 10.で組織を細切する際に、0.5×0.5×0.2cm大の1-2片を別に取り、術中迅速診断用組織標本作製の要領で、凍結組織切片作製用包埋剤(いわゆる Optimal Cutting Temperature [OCT] compound)に包埋し、ドライアイス・アセトン等で凍結し、超低温槽(-80℃)に保管することも推奨される(E)。
注:OCT 包埋標本作製時の氷晶の形成を避けるため、包埋用の組織を一度OCT compoundに浸漬し、新しいOCT compoundで包埋し急速凍結することがすすめられる (E)。
- OCT包埋標本を超低温槽 (-80℃)中で長期保管する際には、パラフィルム等で厳重に包装し密閉性の高い容器に収納する等、試料の乾燥を防ぐように充分留意しなければならない。
注: 乾燥したブロックからは、概して剪断化した核酸しか抽出できない (N)。
注: 良好な条件で長期保管した試料においては核酸の品質は概して保持されているが、解析前に、抽出した核酸の品質検証をブロックごとに行うべきである。[実証データ ⑪]
注: OCT包埋標本から薄切の後HE染色標本あるいは免疫染色標本等を作製して鏡検することにより、研究者に提供する組織の病変細胞 (癌細胞) 含有率の情報を提供することができる。組織標本の鏡検で癌細胞含有率を算出するには、
(a) 対象複数視野の癌細胞数をカウンターを用いて極力正確に計測し、同様に計測した全細胞数で除す方法 (E)と、
(b) 低倍率at a glanceで10%未満、10%以上20%未満、以後10%毎等に大別する方法 (E)
がある。(b)でも有益な知見が得られる場合があり、実行可能性に鑑みて各施設で(a)または(b)を選択するべきである。[実証データ ⑫]
注 OCT包埋標本から薄切の後HE染色標本を作製して組織像を観察し、マイクロダイセクションを実施するか、あるいは未染標本からそのまま核酸を抽出する等して、各種の解析に供すことができる。各種解析に際しては、薄切が反応を利する場合と、包埋剤の混入が反応を阻害する場合がある。特に、OCT compoundが核酸のカラム精製・タンパク質分析等を阻害する場合がある。
OCT包埋標本作製には、組織像を確認できる利点があり、種々の解析が可能であるが、乾燥を防ぐ等管理に細心の注意を要すのみならず、癌細胞含有率評価を含むバンキング作業量が格段と増加する。よって、各施設における実行可能性に鑑みて、充分なコンセンサスが得られた場合にのみOCT包埋標本を作製すべきである。
【研究使用】
- 研究者に試料を提供するため液体窒素保存容器等から試料を取り出す作業は、標準的には用手的に行うが、他の試料への影響を最小限にするため極力手早く作業する (A)。
注: 組織片を収納したチューブはドライアイス上に取り出すなどし、研究者への提供あるいは移送開始まで、極力試料の質を保持するように努める (A)。
- 試料の提供情報・使用量等を、適切な管理アプリケーション等に登録する (A)。
注: 残余組織片・抽出した核酸・解析結果の返納を求めるバイオバンク等においては、使用歴 (研究者・研究課題等)を特に詳細に管理アプリケーション等に記録する (E)。
【移送】
- 長期保管設備を持たない施設等においては、組織を収納したチューブをデュワー瓶中の液体窒素やドライアイス・アセトンに浸漬して十分に凍結した後、液体窒素保存容器を持つ施設等へ適切な手段で移送する。また、遠隔地の研究者に試料を提供する際にも、適切な手段で移送する。
- 通常、温度保持が期待される非密閉移送容器 (簡易的には発泡スチロール容器)にドライアイス等を充填し、冷凍便により運送業者に輸送を委託する (A)。
注: -80℃等の温度保持を保証し、温度記録用のチップを内蔵した移送容器等を用いる生体試料専門運送業者もある (E)。
但し、完全に凍結した組織の数日内の輸送であれば、-80℃等の温度保持を保証する専門運送業者に委託せず、ドライアイス充填発泡スチロール容器を用いた冷凍便等で移送しても、抽出した核酸等の品質の低下は明らかでない。[実証データ ⑬]・[実証データ ⑭]
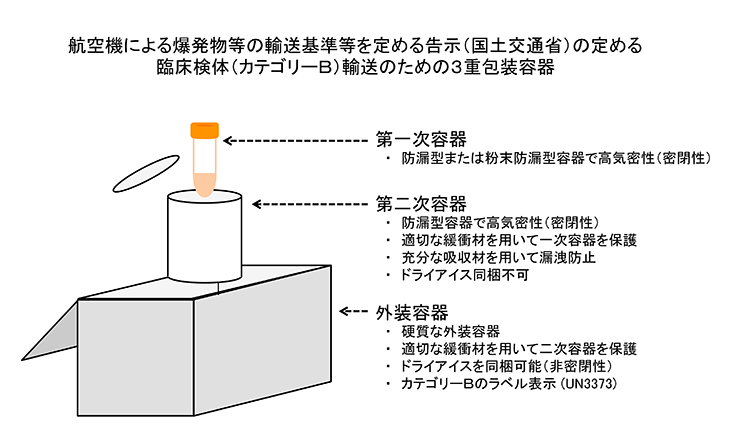
- 世界保健機構(WHO)感染性物質の輸送規則による生物由来物質カテゴリーB (UN3373) (その物質への曝露によって、健康なヒトまたは動物に恒久的な障害や、生命を脅かす様な、あるいは致死的な疾病を、引き起こす可能性のある状態で輸送される感染性物質 [カテゴリーA]ではないヒト由来試料)を航空機により輸送しようとする場合は、「航空機による爆発物の輸送基準等を定める告示 (国土交通省)」の定める3重包装容器を用いなければならない (L)。
【バイオセーフティー】
- 感染性病原体を含むのは一部の症例であるとしても、バンキング実務等を行うことによって暴露の可能性が生じる場合は、実務者に対してリスクとなる。したがって、全ての試料はバイオハザードとして扱うべきである (L)。
- バイオバンクの管理者等は、下記文書等を参照し、安全操作マニュアル等を策定し、全実務者がそれらを確実に理解できるよう配慮する (L)。
- 国立感染症研究所病原体等安全規程
- National Cancer Institute Best Practices Biospecimen Resources June (2007)
- WHO: Biorisk management; laboratory biosecurity guidance (2006)
- OECD: Best practice Guidelines on Biosecurity for Biological Resource Centres(2007)
- 実務者等は安全操作マニュアル等をよく読み、これに従って業務を遂行しなければならない。さらに、管理者等は実務者に適切な実習を提供しなければならない (L)。
注: 具体的には、実験室における一般的な安全管理措置に加え、臨床現場におけるのと同様の予防措置を求める。具体的には、作業中手袋とフェースシールド等を着用し、手洗いを励行する。
注: 特に病理医・病理に関わる臨床検査技師の感染リスクが高い結核の感染予防について充分配慮する。
- 飛沫やエアロゾルによって暴露する可能性がある場合は、国立感染症研究所病原体等安全規程に定めるバイオセーフティーレベル2に準じ、試料の容器を開ける際、安全キャビネット内でこれを行う (L)。
- バイオバンク等の全ての実務者がB型肝炎ワクチン接種等を受けられるようにし、暴露した全ての実務者が暴露後の検査を受け、経過観察され、追跡されるように取りはからわなければならない (L)。
【試料の廃棄】
- 試料提供者から研究利用への同意の撤回があるときなど、病理凍結組織を廃棄する必要がある場合には、手術等に伴って発生する病理廃棄物 (摘出臓器、組織、郭清に伴う皮膚等)と同様に廃棄し、廃棄日・廃棄理由等を管理アプリケーション等に記録する。